
- Autor Daisy Haig haig@petsoundness.com.
- Public 2023-12-17 03:12.
- Ostatnio zmodyfikowany 2025-01-24 12:40.
Firma: Stokes Healthcare Inc.
Nazwa marki: Pilokarpina 0,1% roztwór oftalmiczny
Data wycofania: 13.03.2019
Produkt: Pilokarpina 0,1% roztwór oftalmiczny
Numer partii: R180052
Data ważności: 17 lutego 2019 r.
Produkt służy do leczenia wysokiego ciśnienia wewnątrzgałkowego i jest pakowany w 10 mililitrowe pojemniki z kroplami. Był dystrybuowany w Alabamie, Kalifornii, Kolorado, Connecticut, Delware, na Florydzie, Georgii, Iowa, Idaho, Illinois, Kansas, Kentucky, Luizjanie, Massachusetts, Maryland, Michigan, Północnej Karolinie, New Jersey, Pensylwanii, Wirginii i Waszyngtonie.
Powód wycofania:
Stokes Healthcare Inc. dobrowolnie wycofuje 1 partię 81 jednostek Pilocarpine 0.1% oftalmic Solution, do poziomu konsumenckiego i gabinetu weterynaryjnego. Stwierdzono, że roztwór oftalmiczny zawiera wyższy poziom konserwującego chlorku benzalkoniowego niż typowy.
Oświadczenie o ryzyku: Stosowanie tego produktu może potencjalnie spowodować nieodwracalny zespół suchego oka ze względu na podwyższone stężenie środka konserwującego w tych kroplach do oczu. Suche oko wymaga interwencji medycznej przez całe życie i może prowadzić do bólu i ślepoty, jeśli nie jest leczone. Jeśli Twój zwierzak nadmiernie mruga, obrzęk oka, wydzielina z oka lub inne oznaki podrażnienia oka, skontaktuj się z weterynarzem. Stokes Healthcare przeprowadziło szeroko zakrojone dochodzenie w sprawie tego zdarzenia. Do chwili obecnej firma Stokes Healthcare Inc. otrzymała 8 skarg dotyczących podrażnienia oczu, które jest częstym skutkiem ubocznym stosowania roztworu do oczu pilokarpiny.
Co robić:
Stokes Healthcare Inc. powiadamia swoich klientów listownie i telefonicznie oraz organizuje zwrot i wymianę wszystkich wycofanych produktów. Konsumenci i gabinety weterynaryjne, którzy posiadają 0,1% roztwór do oczu Pilocarpine, który jest wycofywany, powinni natychmiast zaprzestać używania produktu i skontaktować się ze Stokes Healthcare Inc. w celu umówienia zwrotu i wymiany.
Konsumenci z pytaniami dotyczącymi tego wycofania mogą skontaktować się ze Stokes Healthcare Inc. przez telefon (856) 454-3368 lub e-mail pod adresem RHAmara@StokesHealthcare.com poniedziałek-piątek 9:00-19:00 i soboty 9:00-13:00; Wschodni czas standardowy. Konsumenci powinni skontaktować się z weterynarzem swojego pupila, jeśli zwierzę doświadczyło jakichkolwiek problemów, które mogą być związane z przyjmowaniem lub stosowaniem tego produktu leczniczego.
Centrum Medycyny Weterynaryjnej zaleca skontaktowanie się z firmą farmaceutyczną w celu zgłoszenia niepożądanych doświadczeń związanych z lekami lub wad produktów dla produktów zwierzęcych zatwierdzonych przez FDA. Firma farmaceutyczna odpowiedzialna za zatwierdzony produkt jest zobowiązana do przedłożenia tych raportów do FDA. Zadzwoń (856) 454-3316.
- Jeśli wolisz zgłosić się bezpośrednio do FDA, możesz przesłać formularz FDA 1932a, klikając łącze do formularza znajdującego się pod adresem https://www.fda.gov/AnimalVeterinary/SafetyHealth/ReportaProblem/ucm055305.htm i postępując zgodnie z instrukcjami dotyczącymi wysyłania wiadomości e-mail wypełniony formularz do FDA.
- Jeśli masz pytanie dotyczące raportowania ADE lub potrzebujesz papierowej kopii formularza, skontaktuj się z CVM za pośrednictwem poczty elektronicznej AskCVM@fda.hhs.gov lub telefonicznie pod numerem 1-888-FDA-VETS (1-888-332-8387).
Źródło: FDA
Zalecana:
Problemy Z Odżywianiem Zwierząt Purina Dobrowolne Wycofanie Hodowcy Purina Honor Show Chow Showlamb Ze Względu Na Podwyższony Poziom Miedzi

Firma: Odżywianie zwierząt Purina Nazwa handlowa: Purina Honor Show Chow Data wycofania: 12/28/2018 Produkt: Hodowca Purina Honor Show Chow Showlamb (nr partii: 8SEP10WIL1) Numer formuły: 552S Numer przedmiotu: 3004494-506 Produkt: Purina Honor Show Chow Showlamb Hodowca (nr partii: 8SEP18WIL1) Numer formuły: 552S Numer przedmiotu: 3004494-506 Produkt był dystrybuowany w Arkansas, Luizjanie, Oklahomie i Teksasie Powód wycofania: Purina Animal Nutrition
Columbia River Natural Pet Foods Inc. Dobrowolnie Rozszerza Wycofanie, Aby Uwzględnić Ciasto Krowie Oraz Kurczaka I Warzywa Świeże Mrożone Mięso Dla Psów I Kotów Ze Względu Na Możl
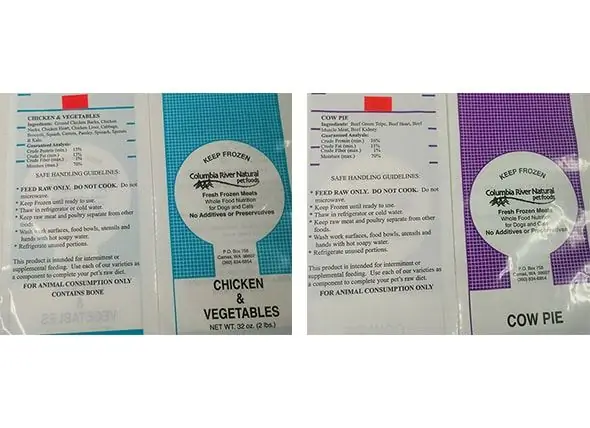
Firma: Columbia River Natural Pet Foods Inc. Data wycofania: 24.12.2018 r. Oba produkty były dystrybuowane na Alasce, w Oregonie i Waszyngtonie za pośrednictwem sklepów detalicznych i dostawy bezpośredniej. Produkt: Cow Pie świeże mięso mrożone dla psów i kotów, 2lbs (261 opakowań) Dostarczany w fioletowych i białych plastikowych torebkach Lot #: 72618 (Znaleziony na pomarańczowej naklejce) Rok produkcji: lipiec 2018 i listopad 2018 Produkt: Kurczak i Warzywa
Wycofanie Z Rynku Karmy Dla Psów Z Kurczakiem I Brązowym Ryżem Wydawanej W Wielu Sklepach Spożywczych Ze Względu Na Podwyższony Poziom Witaminy D

Firma: Sunshine Mills, Inc. Nazwa marki: Obfitość Data wycofania: 12.05.2018 Sklepy King Soopers i City Market Sprzedawane w lokalizacjach w Kolorado, Utah, Nowym Meksyku i Wyoming Produkt: Pełnowartościowa karma dla psów z kurczakiem i brązowym ryżem, 4 funty (UPC: 11110-83556) Kod daty przydatności do spożycia: 11/01/2018-11/16/2019 Produkt: Pełnowartościowa karma dla psów z kurczakiem i brązowym ryżem, 14 funtów (UPC: 11110-83573) Data przydatności do spoż
Przysmaki Kuchenne Milo Dobrowolnie Wycofane Ze Względu Na Potencjalnie Podwyższony Poziom Hormonu Tarczycy

The J.M. Smucker Company ogłosiło, że będzie to ograniczone wycofanie
Odmiany Odżywczej Mokrej Karmy Dla Kotów Dobrowolnie Wycofane Ze Względu Na Podwyższony Poziom Witaminy D

Firma Ainsworth Pet Nutrition z siedzibą w Meadville w stanie Pensylwania wydała dobrowolne wycofanie karmy dla kotów pięciu odmian mokrej karmy dla kotów Rachael Ray Nutrish ze względu na potencjalnie podwyższony poziom witaminy D. Objawy nadmiernego spożycia witaminy D mogą obejmować wymioty lub biegunkę, zwiększone pragnienie i oddawanie moczu oraz drżenie mięśni lub drgawki. Objawy zwykle
